Nouveaux anticoagulants : inventons la SlowPharmacie
Vu de mon cabinet de médecine générale et en parlant avec les collègues, notre expérience (non significative, non représentative, non statistiquement vérifiable) ne semble pas très positive concernant les NACO.
Il s'agit là d'une nouvelle classe d'anticoagulants oraux qui a l'avantage de ne pas nécessiter de prise de sang de contrôle, mais qui a deux inconvénients non négligeables :
- leur coût , autour de 40 euros pour un mois de traitement (dabigatran) contre 2 à 6 euros pour la warfarine (auquel il faut ajouter le coût du contrôle d INR par prise de sang).
- l'absence d'antidote en cas de saignement lié à une surdose ou une hémorragie liée à un choc (vitamine K pour ce qui est de la warfarine).
Nous voyons beaucoup de traitements anticoagulants par AVK changés par les spécialistes lors du contrôle annuel, on peut dire en tout cas que comme les pilules 3G, les généralistes ne sont pas "à la manoeuvre" et sont plutôt circonspects.
Et nous voyons les premières hospitalisations pour iatrogénie, qui nous semblent un peu trop fréquentes (mais encore une fois non significatives statistiquement).
Les questions qui se posent ici sont les mêmes que celles qui ont concerné les glitazones, ou une majorité de traitements innovants récents (pilules 3G) : leurs indications et bénéfices ne sont pas nuls, loin s 'en faut, mais leurs indications, contre indications, effets secondaires sont une fois de plus mal anticipés.
Et la prescription massive à des populations qui n'en tirent pas bénéfice (versus les "vieux traitements") expose à deux choses : un coût inadmissible au vu de l 'absence de bénéfice médical, et des effets secondaires à la mesure de l'explosion des prescriptions injustifiées : si l'on prescrivait 3 grammes d'aspirine par jour a quatre millions de Français, nous aurions une hécatombe.
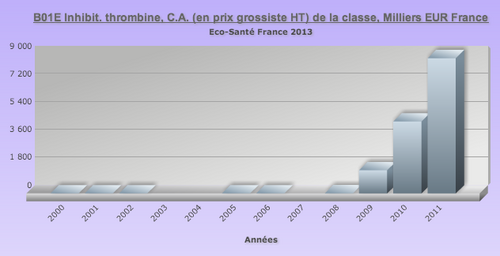
La stratégie des laboratoires est de rapidement "exploser le marché" et réussir à transformer une majorité de vieilles prescriptions d' AVK en prescription de NACO, pour une simple raison : ne pas laisser les concurrents s'implanter, car une fois le changement de traitement vers un NACO réalisé, la retransformation de prescription est incertaine.
Concernant le diabigatran, on constate que la documentation d’accidents cardiaques plus fréquents (+33%) aurait sans doute nécessité une restriction d 'AMM dans un premier temps. (ici aussi). Je ne vois hélas rien à ce sujet de ce coté de l 'atlantique.
Les valves cardiaques sont maintenant aussi clairement une contre indication ( étude REALIGN et décisions FDA/EMA) , ainsi que l 'insuffisance rénale (qui a été prise en compte dès le lancement).
J ai été surpris personnellement par certaines données US, données a posteriori puisqu'émanant des notifications d'accidents à la FDA (et qui contredisent les données rassurantes de RE-LY 2009).
La mortalité par saignement est en effet relevée à 638 contre 44 pour la warfarine 2011/2012 , alors que le nombre de consommateurs de diabigatran est bien moindre.
Et plus récemment, une analyse des données de notification a inspiré cet article.
On y retient 4000 saignements sous diabigatran avec 638 décès contre 800 événements sous warfarine avec 44 décès : le ratio événements sur nombre de décès indique qu'en cas de saignement, ça semble se passer nettement moins bien sans antidote (trois fois plus de décès, 15% contre 5,5%).
Et le nombre absolu semble important car la consommation de diabigatran est bien moindre que celle de warfarine.
Seule une sous notification massive des événements sous warfarine est à même d'expliquer ce différentiel, mais cette explication semble bien fragile.
Allons nous une fois encore assister au retrait de ces nouvelles molécules dans un délai de un an, alors qu'elles ne sont pas inintéressantes ?
La responsabilité n'en revient pas aux chercheurs, mais au circuit de commercialisation, et aux circuits de contrôle sanitaire, qui oublient de donner du temps, et de limiter les indications, exposant massivement des patients qui ne tirent aucun bénéfice de molécules innovantes, puisque déjà bien traités avec de vieux médicaments bien connus (et bien moins coûteux).
Nous assistons à la répétition de cette façon de procéder depuis une dizaine d'années (Coxib , Cerivastatine, Glitazones...).
Il reste donc à inventer la SlowPharmacie, au bénéfice de tous ; et même celui des laboratoires, qui n'auront pas à gérer les aspects juridiques liés a ces lancements chaotiques et effrayants.
Restreindre les indications à des populations ciblées en limitant ainsi le risque est la bonne façon de procéder. C'est aussi redonner du pouvoir aux chercheurs, aux patients et aux soignants, au détriment des marketeurs et des financiers.
En attendant, l’étude de Karen Lasser (2002) reste pleinement pertinente : évitons de prescrire le dernier médicament à la mode !
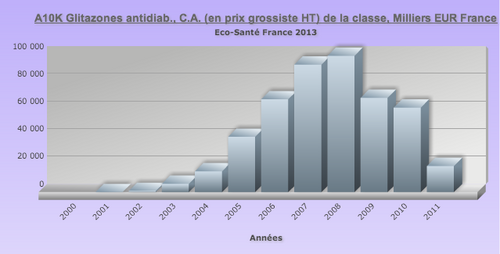
Fast Pharmacie typique : Glitazones : introduction, puis premier chiffre d'affaire dans la classe antidiabétiques oraux, puis retrait (cancers de la vessie, événements cardiovasculaires).
A découvrir aussi
- IGAS : l' apolitique du médicament
- Communiqué de presse de l 'ANSM portant sur le mésusage et les accidents de braguette *
- Médicament générique : qui veut gagner des millions ?
Inscrivez-vous au blog
Soyez prévenu par email des prochaines mises à jour
Rejoignez les 232 autres membres